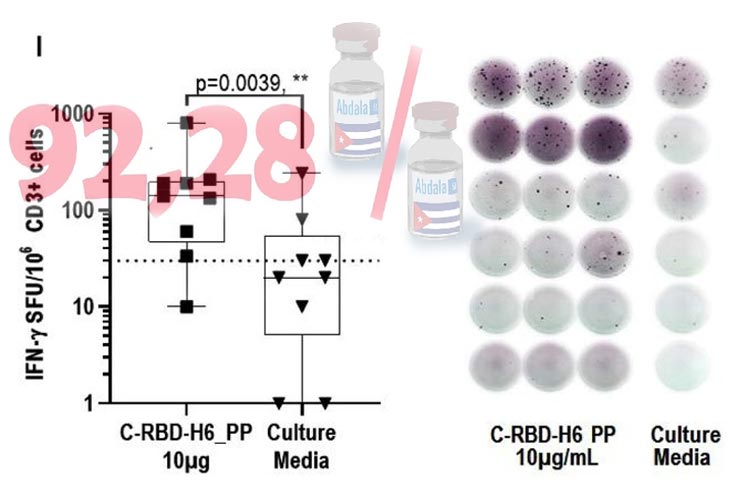
La información divulgada por el Grupo Empresarial de las Industrias Biotecnológica y Farmacéutica de Cuba (BioCubaFarma) en su cuenta en Twitter se refiere a la propuesta desarrollada por el Centro de Ingeniería Genética y Biotecnología (CIGB) que ya demostró un 92,28 por ciento de eficacia en su ensayo clínico fase III luego de administrar sus tres dosis.
La publicación hace referencia al desarrollo de una proteína del dominio de unión al receptor (RBD) del SARS-CoV-2, expresada en la levadura Pichia pastoris, cuyos datos sugieren que es adecuada como candidata a vacuna contra la Covid-19.
El artículo resaltó que esto es parte del esfuerzo por desarrollar vacunas basadas en plataformas tecnológicas económicamente accesibles, lo cual es esencial para extender la inmunización a toda la población mundial y lograr la inmunidad colectiva deseada para poner fin a la pandemia.
Cuba se encuentra en espera de la autorización para uso de emergencia de este candidato vacunal antiCovid-19 por parte de autoridades regulatorias nacionales que analizan la documentación requerida e inspeccionan el proceso productivo.
El Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos analiza el expediente del inyectable y realiza la inspección al proceso productivo, para lo cual se comprueba la elaboración del fármaco en el CIGB y los Laboratorios Aica, con vistas a avalar el cumplimiento de las Buenas Prácticas de Fabricación.
Abdala sobrepasó el límite de eficacia (50 por ciento) establecido por la Organización Mundial de la Salud (OMS) para ser considerada vacuna.
Con la autorización de uso de emergencia los fabricantes de las vacunas contra la Covid-19 pueden solicitar a la OMS el proceso de revisión, que se realiza a través de la evaluación de expertos internacionales.
oda/rbp