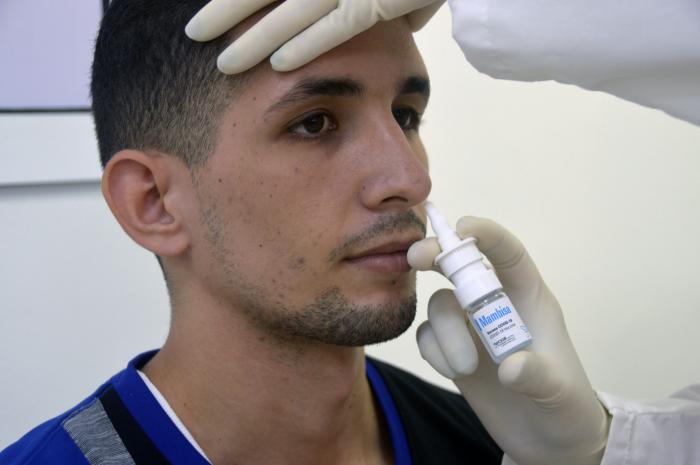
De acuerdo con las declaraciones de Gerardo Guillén, director de Investigaciones Biomédicas del Centro de Ingeniería Genética y Biotecnología, entidad creadora del inmunógeno, hasta la fecha se confirman los resultados obtenidos en la fase I del estudio.
Según refirió al diario Granma, esperan poder cumplir con el plan de presentar a la Autoridad Regulatoria Nacional el informe de la investigación.
El propósito final, dijo, es poder obtener el autorizo de uso de emergencia de este y de la vacuna Abdala como dosis de refuerzo en los convalecientes, es decir, que se puedan utilizar indistintamente cualquiera de ellos.
Eso depende, abundó, de si los dos grupos del estudio cumplan los criterios de éxito, consistente en que los voluntarios incluidos incrementen en al menos cuatro veces sus títulos de anticuerpos, o en un 20 por ciento la capacidad de esos anticuerpos de inhibir al virus SARS-COV-2 en un test analítico de laboratorio.
Afirmó el científico que esperan poder tener los resultados de los análisis en un par de semanas, los cuales serían anunciados en el Congreso Internacional de la Biotecnología Cubana (BioHabana 2022), previsto para celebrarse en la capital cubana del 25 al 29 de abril.
El estudio clínico de Mambisa, que tiene en el Hospital Hermanos Ameijeiras de La Habana se sede principal, se encuentra a punto de terminar la fase II, explicó por su parte la investigadora principal del estudio, Iglemis Figueroa.
Acorde con Figueroa, en la investigación se incluyeron un total de mil 040 sujetos convalecientes, distribuidos en cuatro grupos: dos vacunados con una dosis de refuerzo de Mambisa, y otros dos con una dosis de Abdala.
Si bien el centro hospitalario de la capital fue el único sitio clínico habilitado para el ensayo, luego se hizo necesario abrir sitios en las provincias de Pinar del Río, Camagüey y Santiago de Cuba, reveló.
mem/ifs